Vzteklina z pohledu infektologa
J. Dvořák
Centrum Očkování a cestovní medicíny Avenier, Praha 6
Souhrn
Vzteklina bezpochyby patří mezi nejzávažnější infekční onemocnění vůbec. Jde také o jednu z nejstarších známých chorob člověka. Proti
vzteklině doposud nemáme účin nou kauzální léčbu. I přes všeobecné úsilí o kontrolu této infekce na ni každoročně zemřou desítky tisíc lidí.
Pro cestovatele představuje nákaza vzteklinou reálné nebezpečí a vzhledem k výše uvedeným argumentům toto riziko nelze podceňovat.
Následující text podává ucelený přehled o tomto onemocnění a shrnuje praktické přístupy s důrazem na prevenci.
Klíčová slova
vzteklina – encefalitida – zoonóza – hydrofobie – preexpoziční profylaxe – postexpoziční profylaxe
Historie onemocnění
Vzteklina je známá již velice dlouhou dobu. O onemocnění se zmiňují rukopisy z dávné Mezopotámie, první popis nemoci se objevuje v roce 2 300 př. n. l. [1]. Již staří Egypťané znali přenos vztekliny slinami ze zvířat na člověka. V 1. stol. n. l. se vzteklinou ve svých textech zabývá i Celsus, který přichází i s návrhem postexpozičního zákroku – excize a kauterizace rány po pokousání vzteklým zvířetem. Koncem 19. stol. se vzteklinou zabýval Louis Pasteur, který byl průkopníkem vakcinace proti této nemoci.
Virus vztekliny byl poprvé vizualizován pomocí elektronového mikroskopu v roce 1962 [1,2]. .jpg)
Etiologické agens
Původcem vztekliny je virus, který má typický tvar nábojnice, rozměry jsou cca 180 × 75 nm. Obsahuje jednovláknovou ribonukleovou kyselinu kódující pět proteinů [2]. Taxonomicky je řazen do čeledi Rhabdoviridae, kam vedle rodu Lys savirus náleží dále rody Vesicovirus a Ephemerovirus (virus vezikulární stomatitidy z rodu Vesicovirus příležitostně způsobuje onemocnění člověka a jde také o zoonózu). Virus vztekliny patří do rodu Lyssavirus a je známo sedm jeho genotypů – klasický virus vztekliny a dalších pět genotypů způsobujících onemocnění člověka [2,3]. Jednotlivé genotypy se liší svou distribucí, rezervoáry a patogenezí pro člověka (tab. 1).
Virus je relativně citlivý na okolní podmínky, rychle ho ničí teplota nad 50 °C, UV záření, citlivý je na vysušení a na zmražení. Jeho lipidový obal snadno naruší detergenty (mýdlo), ethanol či roztok jodu. Na druhou stranu při příznivých podmínkách přežívá a je infekční 1– 3 dny a ve tkáních při teplotách kolem 4 °C si zachovává svou infekciozitu po dobu několika týdnů [1,2]..jpg)
Epidemiologie vztekliny
Na vzteklinu podle odhadů zemře ročně ve světě kolem 59 000 lidí, pravděpodobně jsou ale tato čísla podhlášená. Onemocnění se zpravidla vyskytuje u vesnických či městských populací s omezeným přístupem ke zdravotní péči. Mezi oblasti s nejvyšším rizikem nákazy patří Asie a Afrika (obr. 1). Nejpostiženější jsou děti do 15 let věku, které představují asi 40 % případů onemocnění [4].
Vzteklina je zoonóza. Infekce se šíří mezi rezervoárovými živočichy vnitrodruhově (enzooticky) nebo mezidruhově (epizooticky). Člověk se vzteklinou nakazí téměř výhradně pokousáním nemocným zvířetem nebo olíznutím rány, jsou popsány ojedinělé přenosy inhalací kontaminovaného aerosolu v jeskyních hustě osídlených netopýry nebo transplantací rohovky nemocného dárce [1]. Interhumánní přenos nebyl dosud zaznamenán.
Všeobecným úsilím se daří, alespoň v některých částech světa, redukovat riziko nákazy. Očkovací kampaně namířené proti šíření vztekliny mezi psy a divokými šelmami snižují následně riziko přenosu infekce na člověka. Příznivý efekt této snahy je vidět především v Evropě a na amerických kontinentech. Očkovací kampaně mají účinek především na domestifi kovaná zvířata, některé druhy volně žijících zvířat vč. netopýrů stále zůstávají významným zdrojem infekce. Obecně lze říci, že v rozvinutějších zemích, kde je aplikována účin ná kontrola šíření vztekliny mezi psy, převládají jako rizikový rezervoár zvířata divoká.
V Africe a Asii naopak psi představují nejčastější zdroj vztekliny pro člověka. Případy vztekliny u člověka jsou v Evropě vzácné (jde vesměs o importované nákazy) a např. ČR je od roku 2004 vztekliny prostá – rabies free [1].
Patogeneze
Virus je patogen ní pro všechny teplokrevné živočichy, nicméně přenos na člověka byl popsán slinami a pokousáním jen některými druhy větších savců (např. psy, liškami, vlky, mývaly, opicemi) a netopýry. Virus se do slin vylučuje již několik dnů před klinickými projevy onemocnění. Riziko přenosu vztekliny po pokousání zvířetem je mimo jiné dáno množstvím viru vylučovaného slin nými žlázami, což se u různých druhů teplokrevných živočichů liší. Dosud nebyl např. popsán přenos vztekliny na člověka z hlodavce, naopak pokousání vzteklým psem odpovídá za 99 % případů nákazy člověka [1].
Šíření a množení viru v organizmu lze popsat ve čtyřech krocích. Po inokulaci do rány po kousnutí vzteklým zvířetem virus nejprve proniká do vláken příčně pruhovaného svalstva. Zde dochází k první replikaci a zvyšuje se tím lokální virová nálož. Jedině v tomto okamžiku, kdy virus ještě nepronikl do nervové tkáně, lze léčebně zasáhnout a zvrátit jinak infaustní prognózu onemocnění [1].
Po období množení ve svalové tkáni, které může trvat několik dní i měsíců, proniká virus přes neuromuskulární synapse do periferních nervů inervujících infikovanou svalovinu. V nervových vláknech pokračuje replikace a pomocí zpětného axonálního transportu je virus pasivně centripetálně transportován periferním nervstvem do centrálního nervového systému (CNS). Zajímavostí je, že stejného principu šíření využívá i herpes simplex virus a tetanospasmin – tetanický toxin [3].
Přes spinální ganglie, kde k replikaci nedochází, se virus dostává do předních rohů míšních a odtud do celého CNS vč. mozkového kmene a limbického systému. V CNS rychle diseminuje a infikuje prakticky každý neuron. Za zmínku stojí, že i přes dramatické klinické projevy přítomnost viru nevyvolává v mozku výrazné cytopatologické efekty, pravděpodobně interferuje především s neurotransmisí. Patogenetický mechanismus poškození CNS zůstává ne zcela objasněn. Při paralytickém stadiu vztekliny bývá nejvíce poškozena mícha, kde histologicky dominují výrazné zánětlivé změny a nekrotická poškození [3].
Z CNS progreduje šíření infekce centrifugálně vlákny somatické i vegetativní nervové soustavy do tělesných orgánů. Virové partikule (histologicky popisovány jako Negriho tělíska) jsou nalézány v příčně pruhovaném svalstvu, myokardu, ledvinách, pankreatu, rohovce, střevě apod. Nejvýznamnější je však jejich přítomnost ve slinných žlázách a exkrece viru slinami. Virus se ve slin ných žlázách dále množí a proniká na sliznici dutiny ústní skrze senzorická nervová zakončení. Do této doby byl virus prakticky skryt imunitním mechanizmům [3]. K viremii nedochází.
Protilátková a buněčná imunitní odpověď na infekci přichází dosti opožděně. Dokonce není aktivována ani v prvním kroku, tedy v období, kde se virus množí ve svalových vláknech. Virus navíc svým působením negativně ovlivňuje buněčnou imunitu (indukuje apoptózu T lymfocytů). Imunitní reakce tak přichází až s odhalením antigenů při extracelulárním šíření viru, je ale chabá a neschopna zastavit diseminované onemocnění. Z tohoto důvodu nelze sérologii použít jako spolehlivou dia gnostickou metodu [1– 3].
Klinický obraz
Inkubační doba se pohybuje od několika dní až po 19 let. U 50 % lidí se onemocnění manifestuje mezi 30 a 90 dny. Velmi dlouhá inkubační doba může být vysvětlena přežíváním viru v makrofázích. Předpokládá se rovněž přímý vztah mezi typem imunitní reakce u hostitele a klinickou formou vztekliny. U pacientů s dominující buněčnou imunitní odpovědí je větší pravděpodobnost rozvoje excitační formy než paralytické [3].
Klinicky se jedná o polioencefalitidu, akutní virový zánět mozku a míchy. Míra expozice slinám rabického zvířete, četnost, rozsah a lokalizace pokousání je v přímé úměře s pravděpodobností a rychlostí rozvoje onemocnění. U drobného poranění kontaminovaného slinami či kousnutí přes vrstvu oblečení je riziko nákazy menší než při vícečetném pokousání či lokalizaci infikované rány na hlavě [1,3].
Onemocnění zpravidla začíná prodromálními příznaky. Bývají nespecifické a vzhledem k dlouhé inkubační době nemusí být zprvu vzteklina zahrnuta do diferenciální diagnózy. Objevují se zvýšené teploty, cefalea, myalgie, únava a malátnost. Dále se přidávají parestezie v oblasti primárního vstupu nákazy, myoedém, nauzea a zvracení. Mohou se rozvinout poruchy chování – agitovanost, anxieta, spavost. Prodromální stadium trvá zpravidla 2– 10 dní. Asi u 80 % pacientů se rozvíjí excitační stadium vztekliny. Nejvíce bývá postižen mozek – encefalitida, typicky limbický systém, mozkový kmen a mozeček. Typickými příznaky jsou hydrofobie a výbuchy agresivity a agitovanosti. Fenomén hydrofobie je způsoben přemrštěným dráždivým reflexem dýchacích svalů a hypersenzitivitou sliznice [2]. Postižení prožívají bolestivé spazmy při snaze polknout tekutinu, v některých případech se bolestivé tonické křeče polykacího svalstva objevují jen při letmém kontaktu rtů s vodou, pohledem na ni či zaslechnutím tekoucí vody nebo mohou být provokovány pouhým závanem vzduchu (aerofobie). Kvůli poruše autonomního nervového systému a hydrofobii postižený jedinec výrazně sliní. Objevuje se dále hyperventilace se zapojením vedlejších dýchacích svalů. K dalším projevům postižení CNS patří halucinace, zmatenost, delirantní stavy. Dochází k vodní a minerálové dysbalanci, nadměrnému pocení, srdečním arytmiím (jako důsledek postižení mozkového kmene a virové myokarditidy) [3].
Paralytické stadium vztekliny se u člověka rozvíjí méně často, zhruba ve 20 % případů. Rozvine se zpravidla při přenosu nákazy netopýrem a opožděném zahájení postexpoziční profylaxe (PEP) [2]. Probíhá pod obrazem ascendentní chabé paralýzy, dochází k obrnám hlavových nervů a končetin, zácpě a retenci moči. Objevuje se rovněž zmatenost a kvantitativní poruchy vědomí.
Vedle více či méně typických neurologických symptomů se mohou rozvinout i příznaky orgánového postižení – průjem, zvracení, ileus, enteroragie, hypotenze a již zmiňované arytmie. Obě stadia nemoci přechází po několika dnech (zpravidla během 2– 14 dní) do kómatu s následným úmrtím. Příčinou smrti je otok mozku, kardiální a respirační selhání [2,3].
Léčba – postexpoziční profylaxe
Kauzální léčba vztekliny neexistuje. I přes veškeré snahy nelze klinicky rozvinuté onemocnění léčbou zastavit a pacient je odsouzen k téměř jisté smrti. Terapie je symptomatická a paliativní. Doposud bylo popsáno jen několik přeživších, převážně s těžkými doživotními následky. Tzv. Mil lwaukee protokol, uvedení nemocného medikamenty do hlubokého bezvědomí, se ukázal jako nespolehlivý a kontroverzní [5].
Nezbývá než zasáhnout v momentu, kdy se virus množí ve svalových vláknech a nepronikl do nervové tkáně. Replikaci a šíření viru se dá zabránit imunizací – aktivní i pasivní. Celosvětově absolvuje postexpoziční profylaxi odhadem 10 milionů lidí ročně [1]. Světová zdravotnická organizace defi nuje tři stupně závažnosti expozice s doporučeným náležitým postupem profylaxe (tab. 2).
Vedle doporučeného ošetření rány se v profylaxi využívají stávající inaktivované vakcíny aplikované postupně ve čtyřech dávkách. Světová zdravotnická organizace doporučuje následující schéma: jedna dávka ve dnech 0, 3, 7 a mezi 21. a 28. dnem (tzv. Es senské schéma, v ně kte rých literárních zdrojích uváděno celkem pět dávek 0, 3, 7, 14 a 21) nebo dvě dávky v den 0 a dále po jedné dávce 7. a 21. den (tzv. Záhřebské schéma) [4]. U osob s předešlou úplnou preexpoziční imunizací se doporučuje aplikovat dvě posilující dávky inaktivované vakcíny v intervalech 0. a 3. den (tab. 2). Vakcíny od různých výrobců jsou zaměnitelné. Při kontaktu s vysokým rizikem se u nevakcinovaných jedinců podává antirabický humánní nebo koňský imunoglobulin, kterým se infi ltruje rána, a případně zbytek se podává intramuskulárně [6].
PEP je nutné zahájit co nejdříve. Nicméně časné ošetření rány detergenty, virucidními přípravky a případná infiltrace imunoglobulinem jsou klíčové pro zabránění pomnožení viru v místě vstupu infekce [3].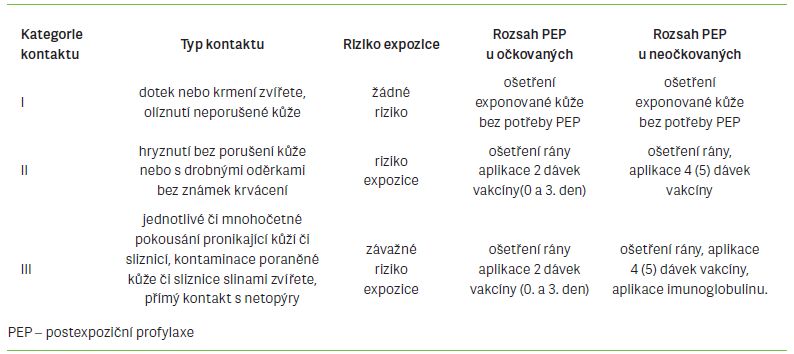
Prevence – preexpoziční profylaxe
U vybraných osob s rizikem nákazy vzteklinou nebo kontaktu se zvířaty je možné a doporučované preventivní očkování – tzv. preexpoziční profylaxe (PrEP). Používají se inaktivované celobuněčné vakcíny, vakcinální kmeny virů jsou připravovány na buněčných kulturách. V současnosti jsou v ČR registrovány dvě vakcíny od různých výrobců: Verorab (virus pomnožený na lidských diploidních Vero buňkách) a Rabipur (k přípravě použity buňky kuřecích embryí). Standardně se očkuje v intervalu: 0., 7. a 21. nebo 28. den. Vzhledem k rychlosti nástupu ochranných protilátek je nanejvýš vhodné, aby poslední dávka PrEP byla aplikována nejpozději 14 dní před vstupem do rizikové oblasti. Vakcinace se považuje za vysoce spolehlivou, do 38 dní po zahájení dosahuje séroprotekce téměř 100 % [6]. Nikdy však k PrEP nelze přistupovat jako ke stoprocentně zaručené ochraně před vzteklinou, tudíž v indikovaných případech je nutné pro všechny případy absolvovat dvě posilující dávky v rámci PEP (tab. 2). To je potřeba cestovateli náležitě zdůraznit.
Indikace k PrEP patří do rukou odborníka na cestovní medicínu, nicméně preventivní očkování lze v zásadě doporučit v následujících situacích [5,7]:
• u cestovatele předpokládáme užší a častý kontakt se zvířaty (domestifi kovanými i divokými) – především z profesionálních důvodů (veterináři, biologové, speleologové apod.),
• cestovatel hodlá z větší části pobývat v přírodě (kempink, trekking) nebo se chystá do odlehlých částí rozvojové země a velmi pravděpodobně bude mít omezený přístup k časné a spolehlivé lékařské péči vč. kompletní PEP,
• dětem cestujícím do rizikových oblastí – děti jsou obecně ve vyšším riziku, mohou postrádat opatrnost v kontaktu se zvířetem, nemusí rozumět varovnému nebo atypickému chování zvířete, je vyšší riziko pokousání do oblasti hlavy,
• dlouhodobé pobyty v zemích se středním nebo vysokým výskytem vztekliny (obr. 1 a 2).
Praktický přístup – prevence a postup po pokousání zvířetem
Při cestách do některých oblastí vzteklina stále představuje neopomenutelné riziko: infaustní prognóza s dramatickým klinickým průběhem, pravděpodobnost opožděné či nesprávně provedené PEP (odlehlé oblasti, rozvojové země se špatným stavem zdravotní péče), riziko nežádoucích účinků vakcín a imunoglobulinu podaných v rámci PEP neskladovaných předtím v optimálních podmínkách. Opožděná nebo neúplná PEP u neočkovaného jedince může mít za následek rozvoj vztekliny [8]. Cestovatel by měl být, vedle očkování, vybaven informacemi, co dělat v případě pokousání zvířetem, a především jak tomu zabránit. Ideální je návštěva centra cestovní medicíny s dostatečným časovým předstihem a konzultace s odborníkem. .jpg)
Pokousání zvířetem představuje komplexnější zdravotní problém než „pouze“ riziko nákazy vzteklinou. Dostatečně poučený cestovatel dokáže efektivně předejít závažným zdravotním problémům. Praktické rady lze shrnout do následujících bodů [7– 9]:
• vyhnout se kontaktu s volně pobíhajícími zvířaty (především psy); v Indii, Thajsku, na Bali a v některých dalších oblastech jihovýchodní Asie je častý kontakt s opicemi – ty nekrmit, v jejich přítomnosti nemanipulovat s jídlem; v jeskyních hustě obydlených netopýry používat ústenku (i z důvodu prevence jiných nakažlivých chorob);
• při pokousání ránu vyčistit, ošetřit mýdlovým roztokem (virus je citlivý na detergenty), dezinfikovat (jodový roztok, alkohol) a krýt (zabránit druhotnému znečištění);
• co nejdříve po pokousání vyhledat lékařské ošetření – rána může být kontaminována bakteriemi z dutiny ústní zvířete; bude možná nutné podat preventivně antibiotika a posilující dávku vakcíny proti tetanu; v některých případech si stav vyžádá chirurgické ošetření (odstranění lacerovaných okrajů rány, šití); dle typu, rozsahu poranění a případné PrEP se zahajuje PEP vztekliny;
• nikdy nepodceňovat možné riziko vztekliny, i zdravě vypadající zvíře může ve svých slinách vylučovat virus v infekční dávce.
MUDr. Jan Dvořák
Centrum Očkování a cestovní medicíny Avenier
Veleslavínská 150/ 44
162 00 Praha 6
Literatura
1. Beneš J (ed). Infekční lékařství. Praha: Galén 2009: 161–165. 2. Cook GC, Zumla AI (ed.). Manson´s Tropical Diseases. 22nd ed. Elsevier 2009: 799–811.
3. Mandell GL, Bennet JE, Dolin R. Principles and Practice of Infectious Diseases. 7th ed. Elsevier 2010: 2249–2253.
4. Rabies vaccines: WHO position paper – April 2018. [online]. Available from: http://www.who.int/rabies/resources/who_wer9316/en/.
5. Beneš J, Kűmpel P, Matouch O. Profylaxe lyssy: Konsensus představitelů infekčních pracovišť v ČR a NRL pro vzteklinu. Klin Mikrobiol Infekc Lek 2003; 9(4): 186–196. 6. Chlíbek R et al. Očkování dospělých. Praha: Mladá Fronta 2018:174–179.
7. Centers for Disease Control and Prevention. CDC Yellow book 2018: Health Information for International Travel. New York: Oxford University Press 2017: 289–291.
8. Maďar R. Ochrana zdraví na cestách. 2 vyd. Martin: Vydavateľstvo Osveta 2014: 85.
9. Keystone JS, Kozarsky PE et al. Travel Medicine. 2nd ed. Elsevier 2008: 465–467.
Zpět na seznam článků

