Virová hepatitida E
P. Macounová, A. Hozák
Ústav epidemiologie a ochrany veřejného zdraví, LF OU Ostrava
Etiologie
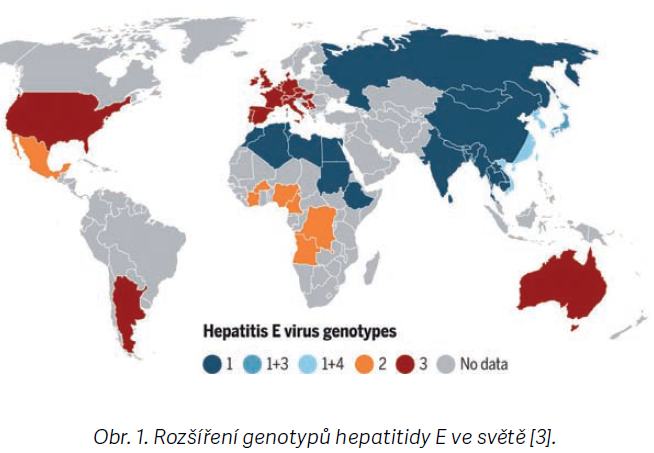
Původcem onemocnění je virus hepatitidy E (HEV), který byl prokázán v roce 1990 elektronovou mikroskopií. HEV je malý neobalený RNA virus o velikosti 27–34 nm, u něhož lze předpokládat vyšší odolnost a schopnost dlouhodobého přetrvání mimo hostitelský organizmus. Taxonomicky ho řadíme do čeledi Hepeviridae, rod Hepevirus [1,2]. Toto členění se ale ukazuje na základě analýz sekvencí HEV u zvířat jako nevyhovující. Pro usnadnění zařazování nově objevených izolátů HEV se navrhuje rozčlenění čeledi na rody Orthohepevirus pro savčí a ptačí a Piscihepevirus pro rybí kmeny. Kmeny viru, které jsou schopné nakazit člověka, se dělí do 4 genotypů. Genotypy se liší geografickým rozmístěním, které je přehledně vyobrazeno na obr. 1 [3], a s tím související odlišnou epidemiologií. Genotypy 1 a 2 se vyskytují výhradně u lidí, a to nejčastěji v rozvojových zemích Afriky, Asie a Střední Ameriky. Genotypy 3 a 4 se vyskytují jak u lidí, tak u zvířat po celém světě, spíše ve vyspělých státech. Existence dalších genotypů je předmětem výzkumu a týká se zatím výhradně zvířecí říše. Předběžně zařazený genotyp 5 má endemický původ v ptačích hejnech, význam infekce pro člověka je nejasný [4,5]. V nedávné době byly u prasat v Japonsku identifi kovány možné 2 nové genotypy 5 a 6, které zatím nebyly prokázány u lidí a jejichž zoonotický potenciál nebyl dosud objasněn [6]. U velbloudů byl popsán genotyp 7 [2]. Všechny genotypy viru náleží pod jeden sérotyp [1,6].
Epidemiologie
Virová hepatitida E je enterálně přenosné onemocnění s poměrně dlouhou inkubační dobou v rozmezí 2–8 týdnů, průměrně 35 dní. Vnímavost k nákaze je všeobecná, imunita po prodělané infekci je pouze krátkodobá, většina osob po prodělané infekci záhy ztrácí protilátky anti-HEV. Před detekováním HEV bylo označováno názvem non-A non-B hepatitida, až důkaz o přenosu fekálně-orální cestou nakažením dobrovolníka ze stolice pacienta v Kyrgyzstánu v roce 1983 vedl k průkazu viru v roce 1990. HEV byla do roku 1996 považována za endemickou infekci v rozvojových zemích, možnost infekce mimo endemické oblasti se zkoumala provedením rozsáhlých séroprevalenčních testů u prasat v roce 1997 ve Spojených státech amerických. Další studie prokázaly souvislost infekcí lidí a rezervoárových zvířat. Virus je rozšířen v chovech prasat domácích i u prasat divokých po celém světě, tudíž prasata jsou považována za významný rezervoár HEV. Riziková je proto konzumace nedostatečně tepelně upraveného vepřového a kančího masa a vnitřností. Nebezpečné je ale i maso jelenovitých zvířat, ryby a mořské plody, v ČR jsou zaznamenány případy alimentární nákazy spojené s konzumací produktů ze zabijaček. Pro spolehlivé zničení viru je třeba zahřátí na 71 °C trvající min. 20 min. V rozvojových zemích je nejčastější příčinou nákazy kontaminovaná voda, která je zejména při záplavách, ale i v souvislosti se špatnými hygienickými podmínkami fekálně znečištěna odpadní vodou a způsobuje rozsáhlé epidemie. Nákaza je možná i vertikálním přenosem z matky na plod během nitroděložního vývoje, přičemž je vysoká pravděpodobnost potratu, narození mrtvého plodu nebo vrozené HEV u dítěte. Dále je možný přenos krevními produkty, kazuistiky popisují i přenos transplantovanými orgány. Zanedbatelný význam má mezilidský přenos, pravděpodobný je zřejmě jen v endemických oblastech během epidemií, jelikož ve stolici je vylučováno jen malé množství viru asi 1 týden před klinickou manifestací a trvá přibližně 2 týdny. Možná je i nákaza přímým kontaktem s infikovaným zvířetem, zejména při manipulaci s ulovenou zvěří a jejím vyvrhováním. Možnému sexuálnímu přenosu HEV nasvědčuje zvýšená prevalence protilátek anti-HEV u homosexuálních mužů, tato možnost však nebyla dostatečně prokázána [1,4,6–8].
Infekce se vyskytuje celosvětově, s převahou v rozvojových zemích. První popsaná epidemie proběhla v Indii v roce 1955, kde se nakazilo přes 29 tisíc lidí, přičemž původně se předpokládalo, že jde o epidemii viru hepatitidy A (HAV), ale retrospektivně se na základě analýz zjistilo, že šlo o epidemii HEV. Podobné epidemie související s pitím kontaminované vody probíhaly v řadě rozvojových zemí, vč. opakovaných epidemií v Indii [6,9]. Nejrozsáhlejší výskyt u více než 100 tisíc osob byl pozorován v letech 1986–1988 v Číně. V současnosti je celosvětově každoročně zaznamenáno nejméně 20 milionů případů, z čehož je přibližně 70 tisíc úmrtí a 3 tisíce mrtvě narozených dětí. Prevalence protilátek vyšší než 25 % je ve Střední Americe, většině Afriky, Asie a na Středním východě [2]. V neendemických oblastech se prevalence protilátek pohybuje mezi 1–3 %, přičemž vyšší prevalence protilátek byla zjištěna u profesně exponovaných osob, jako jsou například veterinární pracovníci, řezníci a pracovníci jatek [7]. Geografické rozšíření HEV je znázorněno na obr. 2 [10].
V ČR byla na základě sérologického přehledu zjištěna prevalence anti-HEV 6,7 % ve věkové skupině 15–64 let, bez rozdílu mezi pohlavími. Při přepočtu na počet osob činí séroprevalence 8,6 %. Nejnižší 3,5 % je u věkové skupiny 15–24 let a stoupá s věkem až na 16,8 % u 55–64letých [11]. Výskyt HEV v ČR se pohybuje v řádu stovek případů a má v posledních letech rostoucí trend, s maximy případů v zimě a na jaře. V minulosti šlo především o importované případy, ale v současné době převažuje autochtonní přenos. Příkladem jsou dvě epidemie z let 2009 a 2011, které proběhly na území Ústeckého kraje, kde onemocnělo 13 a 8 osob po konzumaci vepřového masa a produktů z domácích zabij aček [1,12]. Ve Středočeském kraji proběhla menší epidemie v období od prosince 2011 do února 2012, při které se nakazilo 36 osob, příčinou byla konzumace jitrnic z vepřového masa. V roce 2014 bylo zaznamenáno 52 případů onemocnění s rodinným výskytem v epidemiologické souvislosti. V ČR nejčastěji onemocní muži ve věku 65–69 let, nejčastěji v podzimní a zimní sezóně v souvislosti se zabijačkami. Počet importovaných nákaz klesá, nejčastěji se lidé nakazí HEV v Indii, dále pak v Egyptě, Francii, Itálii a Thajsku. Mortalita HEV dosahuje přibližně 2 %, přičemž podstatně vyšší, až 20 %, může být u těhotných žen, a to zejména ve 3. trimestru [8,13]. 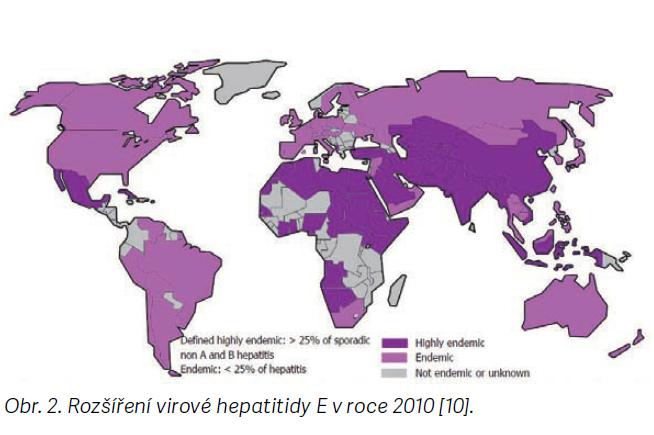
Patofyziologie
Patogenetický mechanizmus HEV se zatím nepodařilo objasnit. Virus poškozuje hepatocyty na podkladě imunitní reakce, podobně jako u HAV. Byly popsány i četné mimojaterní projevy infekce, a to zejména postižení nervového systému, které se objevuje i bez současného poškození jater. Existují nepřímé důkazy o možnosti působení viru přímo na nervovou tkáň. Opakovaná infekce je možná a vyskytují se názory, že může mít závažnější průběh než primoinfekce. K relapsům HEV na rozdíl od HAV nedochází [4,8,14].
Klinický obraz
Klinický průběh onemocnění bývá různě závažný. V rozvojových zemích má infekce těžší průběh s výrazným ikterem. V našich podmínkách nelze nákazu HEV klinicky odlišit od jiných akutních virových hepatitid, ve většině případů probíhá asymptomaticky bez elevace hladiny bilirubinu v séru a jen s nepatrným zvýšením aktivity enzymů alaninaminotransferázy a aspartátaminotransferázy. Mezi typické symptomy patří ikterus trvající 2–4 týdny, tmavá moč, bledá stolice a hepatomegalie čili zvětšená játra. Další popisované příznaky jsou nauzea, zvracení, abdominální diskomfort, snížená chuť k jídlu, zvýšená teplota, tlak v pravém podžebří, celková slabost, vyrážka či bolest kloubů. Akutní hepatitida E většinou samovolně odezní po 6–7 týdnech. Těžší průběh má infekce v těhotenství, což je přirozený stav imunosuprese. Roli zde hrají zejména steroidní hormony a interleukiny, které potlačují imunitní systém a zabraňují regeneraci hepatocytů, což vede ke vzniku poškození nebo až k selhání jater. U pacientů s preexistujícím poškozením jater má HEV rovněž závažnější průběh. Vzácně může akutní průběh u těchto osob vést ke vzniku fulminantní formy hepatitidy, pacienti jsou ohroženi smrtí [1,2,5,15].
Jsou popsány i mimojaterní manifestace jako například pankreatitida pozorovaná pouze v endemických oblastech. Nejčastěji popisované jsou neurologické komplikace jako meningoencefalitida nebo syndrom Guillain-Barré, ale postiženy mohou být rovněž ledviny, krevní elementy či jiné orgány. Na rozdíl od HAV může infekce genotypem 3 HEV přecházet do chronicity u imunosuprimovaných pacientů. Jde zejména o pacienty po transplantacích orgánů, léčené chemoterapií, trpící hematologickou malignitou či HIV pozitivní. S vyšším stupněm poškození imunity stoupá riziko přechodu HEV do chronicity, děje se tak přibližně u 60 % imunosuprimovaných pacientů bez antivirové léčby akutní HEV. V chronickém stadiu virus perzistuje v séru a ve stolici nebo perzistují protilátky imunoglobulinu M (IgM) v séru déle než 6 měsíců společně s elevací jaterních enzymů. U většiny pacientů po odeznění příznaků akutní infekce probíhá chronická hepatitida bezpříznakově. Příznaky u části pacientů mohou přetrvávat, jedná se zejména o ikterus, abdominální diskomfort a únavu. Chronická infekce může vést k cirhóze a selhání jater [1,14].
Diagnostika
Případy HEV nejsou klinicky odlišitelné od jiných typů akutních virových hepatitid. Podezření na toto onemocnění může vzniknout na základě epidemiologických souvislostí, jako je výskyt několika případů v endemických oblastech s rizikem kontaminované vody, v našich podmínkách při rodinném výskytu, po konzumaci rizikových potravin či při těžším průběhu onemocnění u těhotných žen. S konečnou platností je možné diagnózu stanovit na základě výsledků laboratorních vyšetření. Ideální je využít kombinaci sérologických testů a molekulárně biologické metody detekce RNA HEV v biologických vzorcích – ve stolici, krvi, plazmě či séru. Sérologická diagnostika se opírá o průkaz anti-EV protilátek třídy IgM v séru, nejčastěji metodou ELISA. Protilátky IgM se objevují již několik dní před klinickou manifestací a přetrvávají 3–6 měsíců. Současně s IgM následuje i vzestup protilátek třídy imunoglobulinu G (IgG), jejichž nález může sloužit jednak k podpoře specifi city testu, ale především k prokázání prodělaného onemocnění, jelikož anti-HEV IgG protilátky přetrvávají v séru min. rok, často i řadu let po prodělané HEV. Zvýšené hodnoty jaterních enzymů a bilirubinu bývají přítomny v akutní fázi onemocnění. V případě odběru biologického materiálu vzniká problém s načasováním, jelikož po manifestaci onemocnění klesá koncentrace RNA viru v krvi i ve stolici, kde je možná detekce 2–3 týdny po objevení se klinických příznaků. Metodu přímého průkazu RNA HEV v krvi nebo ve stolici, k čemuž slouží vyšetření metodou polymerázové řetězové reakce, je vhodné použít ve sporných případech. Využití molekulárně bio logických metod je rovněž užitečné pro epidemiologické účely, jelikož umožňují analýzu genomu HEV a následné rozdělení a porovnání genomů, což může sloužit ke zjištění vztahů mezi jednotlivými případy [1,6,15].
Léčba
V případech se standardním průběhem je podávána pouze symptomatická a podpůrná léčba v podobě infuzí, antiemetik, analgetik či hepatoprotektiv. Z hlediska závažnosti onemocnění by zřejmě nebyla nutná hospitalizace, avšak v ČR vyplývá její povinnost stejně jako u ostatních virových hepatitid z legislativy. Hospitalizace a léčba je nutná u pacientů s těžkým průběhem onemocnění a u těhotných žen. V těchto případech se k léčbě využívají antivirové léky – ribavirin či pegylovaný interferon alfa. Léčba ribavirinem vede ke zmírnění klinických projevů a k poklesu viremie, ale z důvodu jeho teratogenních účinků je jeho použití vyloučeno u těhotných žen. Stejná léčba se podává v případě chronické infekce HEV, u pacientů po transplantacích je rovněž vhodné snížit dávku imunosupresiv, což samo o sobě vede přibližně u 30 % k odeznění chronické infekce [1,6,15–17].
Prognóza
V nekomplikovaných případech u imunokompetentních osob je prognóza většinou dobrá. Komplikovaný průběh je pozorován u těhotných žen, kde infekce může vést až k akutnímu selhání jater. U imunokompromitovaných pacientů je možný přechod do chronicity, u kterých lze pozorovat rychlou progresi vedoucí až k jaterní cirhóze. V případech, kdy je léčba těžkého průběhu bez efektu, je nutné kontaktovat transplantační centrum [1,6,16].
Prevence
Mezi základní metody prevence patří dodržování osobní hygieny. Zejména důležité je kvalitní zásobování pitnou vodou, zvláště při cestování do endemických oblastí je důležité důsledně dbát na pití a používání pouze nezávadné pitné vody, podobně jako u HAV. V našich podmínkách je nejvyšší riziko nákazy z potravin, zejména z vepřového masa a divočiny. Základem prevence je tedy dodržování technologie výroby, distribuce, zpracování masných výrobků a konzumace pouze dostatečně tepelně upraveného masa a vnitřností, zejména při domácích zabijačkách. Ohroženi jsou myslivci manipulující s ulovenou zvěří, měli by proto dodržovat zásady hygieny rukou, případně použít latexové rukavice. Všechny nástroje používané při porcování a úpravě syrového masa by měly být řádně umyty, aby nedošlo ke kontaminaci potravin určených k přímé spotřebě či potravin již tepelně opracovaných. Rizikovým osobám, jako jsou imunosuprimovaní pacienti s chronickým onemocněním jater a těhotné ženy, se nedoporučuje cestování do zemí s endemickým výskytem HEV.
Očkování v Evropě zatím není dostupné. Na vývoji vakcín se pracuje, v roce 2007 byla klinicky testovaná vakcína v Nepálu, její vývoj byl ale z finančních důvodů pozastaven. Od roku 2012 je v Číně klinicky schválena subjednotková vakcína Hecolin© obsahující rekombinantní kapsidový protein z genotypu 1. Ochrana před akutní infekcí HEV genotypu 1 dosahuje podle studie 94–100 %, prokázána byla také zkřížená ochrana proti genotypu 4. Zda je vakcína účinná i proti genotypu 3, který je nejběžnější v Evropě, se zatím nepodařilo potvrdit [1,8,14,16,18].
Literatura
1. Mihalčin M, Polák P, Husa P. Hepatitida E – přehled současných poznatků. Epidemiol Mikrobiol Imunol 2015; 64(2): 72–78.2. Prospere R. Hepatitis E. Medscape 2016. [online]. Available from: https://emedicine.medscape.com/ article/ 178140-overview#showall.
3. Kupferschmidt K. Europe’s new hepatitis problem. Science 2016. [online]. Available from: http://www.sciencemag.org/cgi/doi/10.1126/science.353.6302.862.
4. Beneš J (ed). Infekční lékařství. Praha: Galén 2009.
5. Ehrmann J, Hůlek P et al. Hepatologie. 2. vyd. Praha: Grada 2014.
6. Kubánková M, Němeček V, Chalupa P et al. Virus hepatitidy E. Epidemiol Mikrobiol Imunol 2016, 65(1): 4–14.
7. Göpfertová D, Pazdiora P, Dáňová J. Epidemiologie: obecná a speciální epidemiologie infekčních nemocí. 2. vyd. Praha: Karolinum 2013.
8. Príkazská M., Beneš Č. Virová hepatitida E v ČR. Státní zdravotní ústav 2015. [online]. Dostupné z: http://www.szu.cz/uploads/documents/ CeM/ Zpravy_EM/ 24_2015/ 02_unor/ 63_vir_hep_E.pdf.
9. Trmal J, Beneš Č, Trnková M. Odlišnosti výskytu virových hepatitid A a E v České republice. Epidemiol Mikrobio l Imunol 2013; 62(1): 19–25.
10. Jefferies M, Rauff B, Rashid H et al. Update on global epidemiology of viral hepatitis and preventive strategies. World J Clin Cases 2018; 6(13): 589–599. doi: 10.12998/wjcc.v6.i13.589.
11. Němeček V, Butovičová P, Malý M et al. Prevalence protilátek proti viru hepatitidy E v České republice – sérologický přehled. Epidemiol Mikrobio l Imunol 2017; 66(1): 3–7.
12. Trmal J, Pavlík I, Vašíčková P et al. Epidemie virové hepatitidy E v České republice? Epidemiol Mikrobiol Imunol 2012; 61(1–2): 15–20.
13. Husa P. Virové hepatitidy A a E. Med praxi 2013; 10(2): 78–80.
14. Mihalčin M, Fašeneková L, Husa P. Aktuální pohled na epidemiologii a přístupy k léčbě virových hepatitid A a E. Klin Farmakol Farm 2017; 31(1): 15–18.
15. Hepatitis E. World Health Organization 2018. [online]. Available from: http://www.who.int/en/news-room/ factsheets/detail/ hepatitis-e.
16. Hůlek P, Urbánek P. Hepatologie. 3. vyd. Praha: Grada Publishing 2018.
17. Vyhláška č. 306/ 2012 Sb. Zákony pro lidi. [online]. Dostupné z: https://www.zakonyprolidi.cz/cs/2012-306.
18. Göpfertová D, Pazdiora P et al. 100 infekcí (epidemiologie pro praxi). Praha: Triton 2015.
Mgr. Petra Macounová
Ústav epidemiologie a ochrany veřejného zdraví
LF OU
Syllabova 19
703 00 Ostrava

