Tuberkulóza jako stálá hrozba
A. Pernicová
Centrum Očkování a cestovní medicíny Avenier, Praha
Souhrn
Tuberkulóza patří i v 21. století k největším zabijákům lidské populace. Ve vyspělých zemích, vč. ČR, je však její výskyt poměrně nízký. Tato skutečnost společně s vyšší reaktogenitou vakcíny a nižší efektivitou BCG vakcíny vytvořené metodou starou cca 100 let vedla ke zrušení povinného očkování proti TBC na našem území. Očkování je však stále hlavní možností, jak zabránit závažným formám choroby a šíření nemoci v populaci. V současné době je proto věnováno velké úsilí vývoji bezpečnější a účinnější očkovací látky, než je dosud užívaný preparát. Velké naděje jsou vkládány zejména do vyvíjené dánské vakcíny, která naučí imunitní systém rozeznat specifické proteiny bakterie, a zabrání jí tak vyhnout se přirozeným obranným mechanizmům organizmu.
Klíčová slova
tuberkulóza – TBC – BCG – Mantoux test – PPD – vyhláška – prevence – vakcína – očkování
Úvod
Tuberkulóza (TBC) je infekční onemocnění způsobené bakterií Mycobacterium tuberculosis (MT). Nemoc provází člověka již staletí, příznaky plicní TBC popsal již Hérodotos ve 4. století před naším letopočtem. Objev jejího původce je spjat se jménem Roberta Kocha, který tuto acidorezistentní tyčku popsal v r. 1882. Bakterie se dodnes na počest svého objevitele někdy označuje jako Kochův bacil [1].
TBC postihuje především plicní tkáň, mohou se však vyskytnout i infekce urogenitálního traktu, lymfatických uzlin, mozkových blan, kostí vč. obratlů (tzv. malum Potti), kůže (lupus vulgaris).
Zdrojem infekce je jedinec s aktivní TBC (typicky s její plicní formou), který vykašlává do svého okolí bakterie MT. Přenos infekce je možný nejen respirační cestou, ale např. i kontaminací otevřené rány mykobakteriemi, pravděpodobnost nákazy je však daleko menší.
Základy diagnostiky
Pro stanovení diagnózy je rozhodující přímý průkaz patogenu mikroskopicky a kultivačně, významnou roli hrají též zobrazovací metody. Tuberkulinový test (též Mantoux II test či PPD – purified protein derivative) lze využít v diagnostice latentní formy TBC.
Jedná se o kožní zkoušku, principem je intradermální aplikace tuberkulinu (nejčastěji do volární strany levého předloktí) a sledování vzniku indurace kůže v místě vpichu po 48– 72 hod. Výsledky testu musí být hodnoceny zkušeným personálem velmi pečlivě. Ke správnému posouzení je totiž nutno vzít v úvahu míru rizika předchozí expozice MT.
Indurace velikosti 5– 10 mm znamená nejčastěji imunitu po očkování, reakce větší než 15 mm je známkou přítomnosti senzibilizovaných T lymfocytů (čtvrtý, tzv. opožděný typ hypersenzitivní reakce), který je typický právě pro latentní TBC.
Mantoux II test odhaluje stupeň hypersenzitivity vůči tuberkulinu. Tuberkulin je čirá kapalina tvořená čištěnými proteiny vybraných kmenů bakterie MT [2]. Velikost indurace nekoreluje s pravděpodobností přítomnosti aktivní TBC ani s imunitou po proběhlé TBC infekci, odpovídá ale pravděpodobnosti rozvoje onemocnění TBC v budoucnu v případě latentní formy nákazy.
Pokud v místě vpichu tuberkulinu vznikne puchýřek, bula, vřed, nekróza či lymfangoitida, značí to vyšší stupeň senzitivity vůči tuberkulinu, a tedy i přítomnost bakterií MT v organizmu.
Indurace velikosti 5 a více mm je pozitivní u lidí v nedávném kontaktu s nemocným TBC, u HIV pozitivních, u lidí s nodulárními či fibrotickými změnami na rentgenovém snímku hrudníku odpovídajícímu známkám po vyléčené TBC, u jedinců po transplantaci orgánů a jiných imunosuprimovaných pacientů vč. těch, kteří užívají vysoké dávky kortikoidů, u pacientů v konečné fázi selhávání ledvin.
Kožní reakce velikosti 10 a více mm je považována za pozitivní u osob po návratu ze zemí s vysokou prevalencí TBC, u injekčních uživatelů drog, u obyvatel a pracovníků ve vysoce rizikovém prostředí (věznice, pečovatelské domy apod.), u laboratorního personálu, který přichází do styku s mykobakteriemi, u pacientů s diabetem, leukemií, chronickým malabsorbčním syndromem aj., u dětí do čtyř let a dále u dětí a mladistvých v kontaktu s vysoce rizikovými dospělými.
Indurace o průměru 15 a více mm je považována za pozitivní (tedy odhaluje latentní TBC) u jedinců bez známého rizika expozice MT. Takto velká kožní reakce už nebývá jen důsledkem předchozí kalmetizace nebo přítomností mykobakterií v okolním prostředí.
Mantoux II test má nízkou senzitivitu i specificitu, může tedy být falešně pozitivní (např. přítomností infekce způsobené netuberkulózními mykobakteriemi nebo po předchozím očkování BCG vakcínou) i falešně negativní (např. při nesprávné technice podání tuberkulinu, jako projev kožní anergie, u velmi čerstvé či naopak dávné infekci TBC, u dítěte do šesti měsíců věku, po nedávné aplikaci živé vakcíny aj.) [2,3].
I přes svou nízkou specificitu se tuberkulinový test v praxi stále provádí např. u zdravotníků, kteří přišli do kontaktu s pacientem, u něhož byla prokázána TBC. Výsledek PPD testu bývá požadován též od našich občanů, kteří jedou studovat či pracovat do zahraničí, např. do Spojených států amerických. Tuberkulinová zkouška také musí být provedena u všech jedinců starších šesti týdnů, u kterých se plánuje očkování proti TBC [3]. Test provádějí kalmetizační centra a plicní kliniky.
Před plánovaným tuberkulinovým testem by min. 4 týdny neměla být podána živá vakcína (viz výše uvedené riziko falešně negativního výsledku) [3].
Dražší, ale citlivější diagnostickou metodou latentní TBC je Quanti-FERON TB Gold test. Toto imunohistochemické vyšetření je založeno na průkazu interferonu gama v krvi vyšetřovaného, která se inkubuje se specifickými antigeny MT. Interferon gama je produktem aktivovaných T lymfocytů jako projev opožděného typu hypersenzitivity – stejně jako u Mantoux II testu [4]. Na rozdíl od něj však výsledek není ovlivněn event. předchozím očkováním proti TBC.
Výskyt TBC ve světě a v ČR
Za r. 2014 bylo diagnostikováno 9,6 milionů nových případů TBC, z toho 1 milion u dětí. Z celkového množství nových případů je 12 % onemocnění TBC zjištěno u současně HIV pozitivních pa cientů, 75 % z toho na africkém kontinentu [5]. Dle CDC (Centers of Disease Control and Prevention) je bakterií infikován každý třetí člověk na planetě. Zejména při dlouhodobých pobytech v cizině jsou pak i naši občané vystaveni vyššímu riziku infekce.
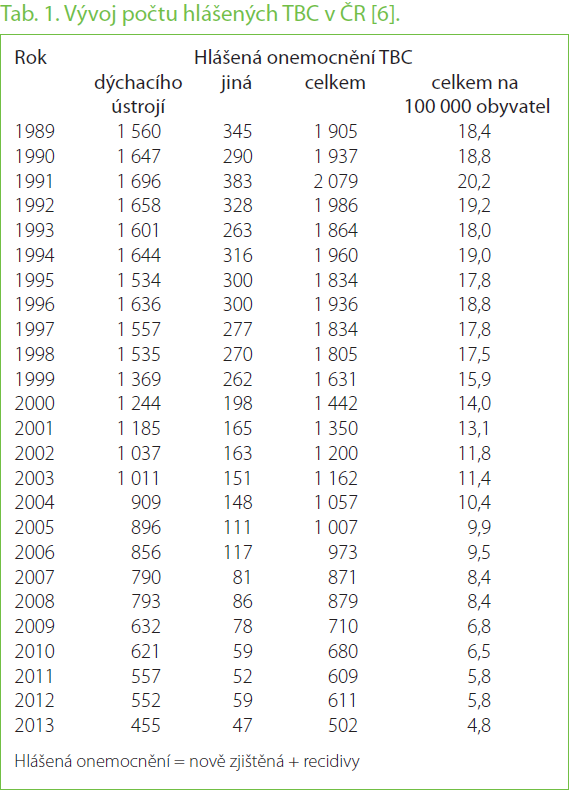
V ČR dochází k trvalému poklesu počtu hlášených případů TBC. Ještě v r. 1992 byla incidence 11,8 případů na 100 000 obyvatel, každoročně následně klesala až na 4,8/ 100 000 v r. 2013 (tab. 1) [6]. Těmito hodnotami se řadíme k zemím s nejnižším výskytem TBC ve světě. Situace se však může změnit v souvislosti s migrací cizinců do naší země.
Pro ilustraci uvádím graf, který znázorňuje záchyt TBC v r. 2013 v ČR podle jednotlivých infi kovaných orgánů (graf 1).
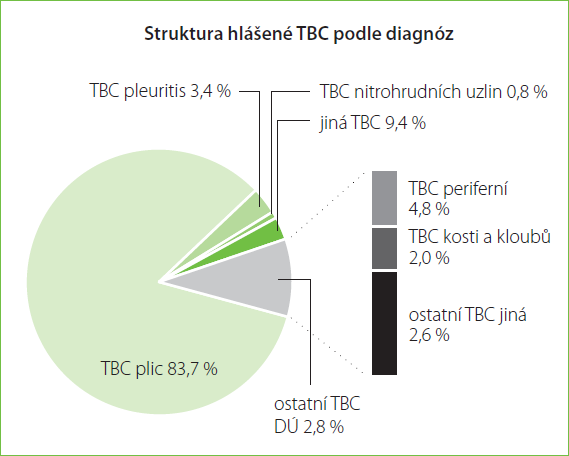
Graf 1. Tuberkulóza v ČR dle postižených orgánů [6]
Proč se u nás neočkuje proti TBC?
Výše zmíněný pokles výskytu TBC v naší zemi vedl v r. 2010 k významné změně. Vyhláškou č. 229/ 2010 Sb., bylo s platností od 1. listopadu 2010 zrušeno pravidelné očkování novorozenců proti TBC. Do té doby se očkování proti TBC, tzv. kalmetizace, provádělo od r. 1953 [7].
Podle výše uvedené vyhlášky se nyní očkují jen děti z rizikových skupin. Doporučení k očkování v kalmetizačním centru v tomto případě vydává pediatr na základě dotazníku vyplněného v porodnici zákonnými zástupci dítěte (tab. 2). Lze očkovat též na přání rodičů, např. při plánovaném dlouhodobém pobytu dítěte v zemi s vyšší incidencí nemoci. K očkování proti TBC se užívá kmen BCG (bacil Calmette-Guérin), který vznikl z plně virulentního kmene Mycobacterium bovis. Francouzský lékař Albert Calmette a veterinář Camille Guérin v r. 1921 opakovaným pasážováním kmene dosáhli jeho oslabení tak, aby mohl být využit k vakcinaci.
Již v období 1986– 1993 byla v ČR ve třech krajích kalmetizace u nerizikových dětí dočasně zrušena. Tento experiment však vedl jednak k opětovnému zvýšení výskytu TBC, navíc se objevily případy aviární mykobakteriózy. Z tohoto důvodu byly neočkované děti doočkovány a vakcinace poté pokračovala až do r. 2010 [7– 9].
K očkování dětí v ČR se léta využívala dánská BCG – VACCINE BEHRING, v současné době je k dispozici pouze polský preparát (Szczepionka Przeciwgruźlicza BCG 10 fi rmy Biomed). Po rekonstituci je toto balení určeno k okamžité aplikaci 10 očkovacích dávek. Pro země, které stále očkují své novorozence plošně (Polsko, Rumunsko aj.) tato skutečnost nepředstavuje problém. Naopak v ČR, kde je očkování dětí z výše uvedeného důvodu spíše výjimečné, vzniká otázka, co s nevyužitými kusy vakcín po otevření balení. Dle informací Státního ústavu pro kontrolu léčiv lze za správných podmínek naředěnou vakcínu uchovat a použít pouze následující 4 hod.
Důvodem zrušení plošné kalmetizace v ČR v r. 2010 je nízká incidence nemoci u nás, ale i to, že se další pravidelná očkování musela odkládat až do zhojení jizvy po kalmetizaci, tj. i několik měsíců. Dítě pak bylo vnímavé delší dobu např. vůči černému kašli. Také možné nežádoucí účinky této technologicky starší vakcíny hrály svou roli v diskuzích ohledně zrušení kalmetizace či jejího přesunu do pozdějšího dětského věku [8]. Vzhledem k tomu, že se jedná o živou vakcínu a děti se očkovaly již čtvrtý den po narození, mohla vést kalmetizace v případě zatím nerozpoznaného imunodeficitu u novorozence k nebezpečným komplikacím. Nejzávažnější z nich je tzv. BCG-itis. Vzniká jako diseminovaná infekce u dětí s primárním imunodeficitem v návaznosti na transplantaci krvetvorných buněk na principu imunitní rekonstituce (obr. 1) [8,10,11].
Méně závažné, ale velmi nepříjemné, jsou např. protrahované hnisavé komplikace kůže či uzlin po očkování. Očkování navíc nechrání před primárním onemocněním plic, brání hematogennímu rozsevu (miliární TBC) a závažné mozkové formě nemoci. Ochrana očkováním trvá asi 10– 20 let, nejúčinnější je tehdy, pokud se očkují malé děti, s rostoucím věkem efekt vakcíny klesá. Revakcinace nemá význam [12,13].
Naopak k výhodám kalmetizace patří současná ochrana i proti infekcím způsobeným netuberkulózními mykobakteriemi (Mycobacterium avium complex). V důsledku zrušení plošného očkování proti TBC se v současné době potýkáme s nárůstem těchto mykobakterióz u dětské populace.

Nová vakcína
TBC ročně zahubí 1,4 milionů lidí na celém světě, vědci proto nevzdávají snahu o vývoj nové vakcíny. Ta by měla být především bezpečnější, ale též účinnější, zejména u dospělých.
Základními cíli jsou [14]:
- Prevence infekce docílená provedením očkování u co nejmenších dětí ještě předtím, než by mohlo dojít k expozici MT.
- Prevence onemocnění, tedy možnost vakcinace jak jedinců po kontaktu s nemocným TBC, tak i těch lidí, kteří jsou infikováni, ale jsou asymptomatičtí. Ochrana před manifestací nemoci by zabránila přenosu infekce v populaci.
- Prevence recidiv TBC. Vakcinace pacientů s vyléčenou TBC by fungovala jako prevence reaktivace nemoci a dalšího možného šíření infekce.
Problémem při vývoji vakcíny je, že MT se dokáže před imunitním systémem dobře „schovávat“, obrana musí být zprostředkovaná aktivovanými T lymfocyty. Protilátková imunita v případě TBC nehraje větší roli.
MT je výborně adaptováno na dlouhodobé přežívání v lidském těle, aniž by s tím imunitní systém mohl cokoli dělat. Proto bylo očkování proti TBC dosud tak problematické. V r. 2014 však dánští vědci přišli s novinkou. Nová vakcína zatím byla testována pouze na myších, výsledky jsou však slibné. Jejich vakcína naučí imunitní systém rozeznat specifické proteiny bakterie, která tak má méně možností, jak se vyhnout přirozeným obranným mechanizmům organizmu. Díky tomu by vakcína dokázala zachránit miliony lidských životů [13].
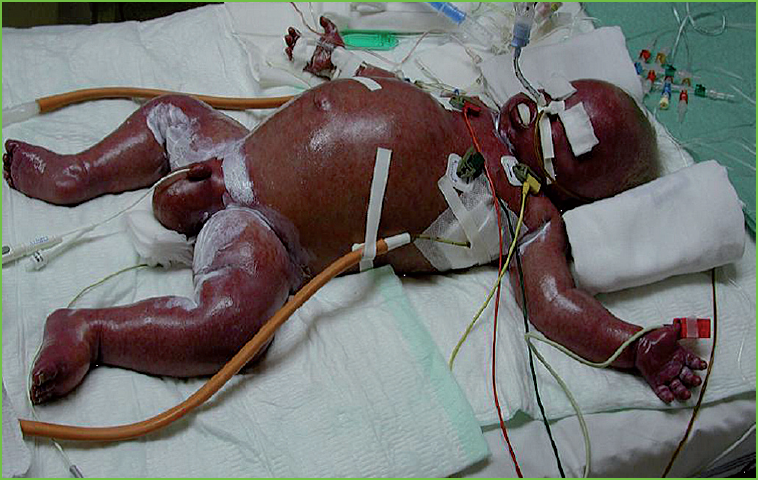
Obr. 1. BCG-itis vzniklá po transplantaci krvetvorných buněk u novorozence s primárním imunodeficitem SCID (severe combined immunodeficiency syndrom) [11]
Závěr
I přes jisté problémy s vakcinací proti TBC je očkování stále hlavní možností, jak zabránit závažným formám choroby a šíření nemoci v populaci. V současné době je věnováno velké úsilí vývoji bezpečnější a účinnější očkovací látky, než je dosud užívaný preparát obsahující BCG.
Literatura
1. Beran J, Havlík J et al (eds). Lexikon očkování. 1. vyd. Praha: Maxdorf s.r.o. 2008.
2. Surajit N, Acharjya B. Mantoux test and its interpretation. Indian Dermatol Online J 2012; 3(1): 2– 6.
3. Centers for Disease Control and Prevention [online]. Available from: http:/ / www.cdc.gov/ tb/ publications/ factsheets/ testing/ skintesting.htm.
4. Abdel-Sameaa SA, Ismail YM, Fayed SM. Comparative study between us ing Quanti-FERON and tuberculin skin test in dia gnosis of Mycobacterium tuberculosis infection. Journal of Chest Diseases and Tuberculosis 2013; 62(1): 137– 143.
5. WHO Library Cataloguing-in-Publication Data Global tuberculosis report 2015 [online].
1. Tuberculosis – epidemiology, 2. Tuberculosis, pulmonary – prevention and control.
3. Tuberculosis – economics. 4. Tuberculosis, multidrug-resistant. 5. An nual reports. I. World Health Organization.
6. Tuberkulóza a respirační nemoci 2013. ÚZIS ČR 2014.
7. Svobodová J. Vakcinační kmen Mycobacterium bovis BCG a očkování proti tuberkulóze [online]. Dostupné z: http:/ / www.szu.cz/ uploads/ documents/ CeM/ Zpravy_EM/ 23_2014/ 05_kveten/ 182_vakcinacni_kmen.pdf.
8. Thon V. Nutnost posunu BCG vakcinace – poučení z komplikací a úmrtí dětí s vrozenými imunodefi ciencemi. Alergie 2010; 12(1): 26– 30.
9. Trnka L, Danková D, Svandová E. Six years‘ experience with the discontinuation of BCG vaccination. 4. Protective eff ect of BCG vaccination against the Mycobacterium avium intracel lulare complex. Tuber Lung Dis 1994; 75(5): 348– 352.
10. Al-Mousa H. An infant with dis seminated bacil lus Calmette-Guerin infection (BCGitis). Internat J Pediatr Adolesc Med 2014; 1(2): 89– 92.
11. BCG-itis po transplantaci krvetvorných buněk u novorozence s primárním imunodefi - citem [online]. Dostupné z: http:/ / imunologie.lf2.cuni.cz/ soubory_esidworkshop/ ESID09_Thon.pdf.
12. Roy A, Eisenhut M, Har ris RJ et al. Eff ect of BCG vaccination against Mycobacterium tuberculosis infection in children: systematic review and meta-analysis. BMJ 2014; 349: g4643.
13. New type of tuberculosis vaccine developed [online]. Available from: http:/ / sciencenordic.com/ new-type-tuberculosis-vaccine-developed.
14. WHO: Im munization, vaccines and bio logicals [online]. Available from: http:/ / www.who.int/ im munization/ research/ development/ tuberculosis/ en/ .
MUDr. Eva Pernicová
Centrum Očkování a cestovní medicíny Avenier
Poliklinika DAM, s.r.o.
Stamicova 21/ 1968, 162 00 Praha 6

